Оглавление
- Дисперсные системы на ЕГЭ
- Что такое дисперсная система?
- Классификация дисперсных систем по дисперсности
- Классификация дисперсных систем по агрегатному состоянию
- Коллоиды и кристаллоиды. Истинные и коллоидные растворы
- Классификация коллоидных систем
Дисперсные системы на ЕГЭ
В кодификаторе, предложенном ФИПИ для 2022 года по химии, в разделе «Химия и жизнь» (пункт 4.1.2) появились следующие темы:
- Дисперсные системы
- Понятие о коллоидах (золи и гели)
- Истинные растворы
В каких заданиях появятся данные понятия пока неизвестно, возможно, это будут задания линии 25.
Что такое дисперсная система?
Дисперсные системы – это измельченные тела одного вещества, равномерно распределенные в сплошной массе другого вещества. Другими словами – это смеси мельчайших частиц, не взаимодействующих друг с другом химически, но имеющие отличные от отдельно взятых чистых веществ, из которых состоит данная система, физические свойства.
Дисперсные системы состоят из двух основных структур:
Дисперсная фаза – частицы, равномерно распределенные в какой-либо среде.
Дисперсионная среда – вещество, в котором растворяют (размешивают) дисперсную фазу.
К дисперсным системам относят большое количество биологических объектов: почву, кровь, цитоплазму, яичный белок и т. д.
Классификация дисперсных систем по дисперсности (размеру частиц)
- Грубодисперсные системы содержат относительно крупные частицы радиусом от 10‒4 до 10‒7м, то есть самые крупные частицы этой системы достигают радиуса 0,1мм.
- Коллоидно-дисперсные системы (золи) содержат частицы с радиусами от 10‒7 до 10‒9 м, то есть самые крупные частицы этих систем достигают радиуса 0,0001мм.
- Молекулярные и ионные растворы (истинные растворы) содержат частицы с радиусом менее 10‒9 м или 0,000001 мм.
Классификация дисперсных систем по размеру частиц
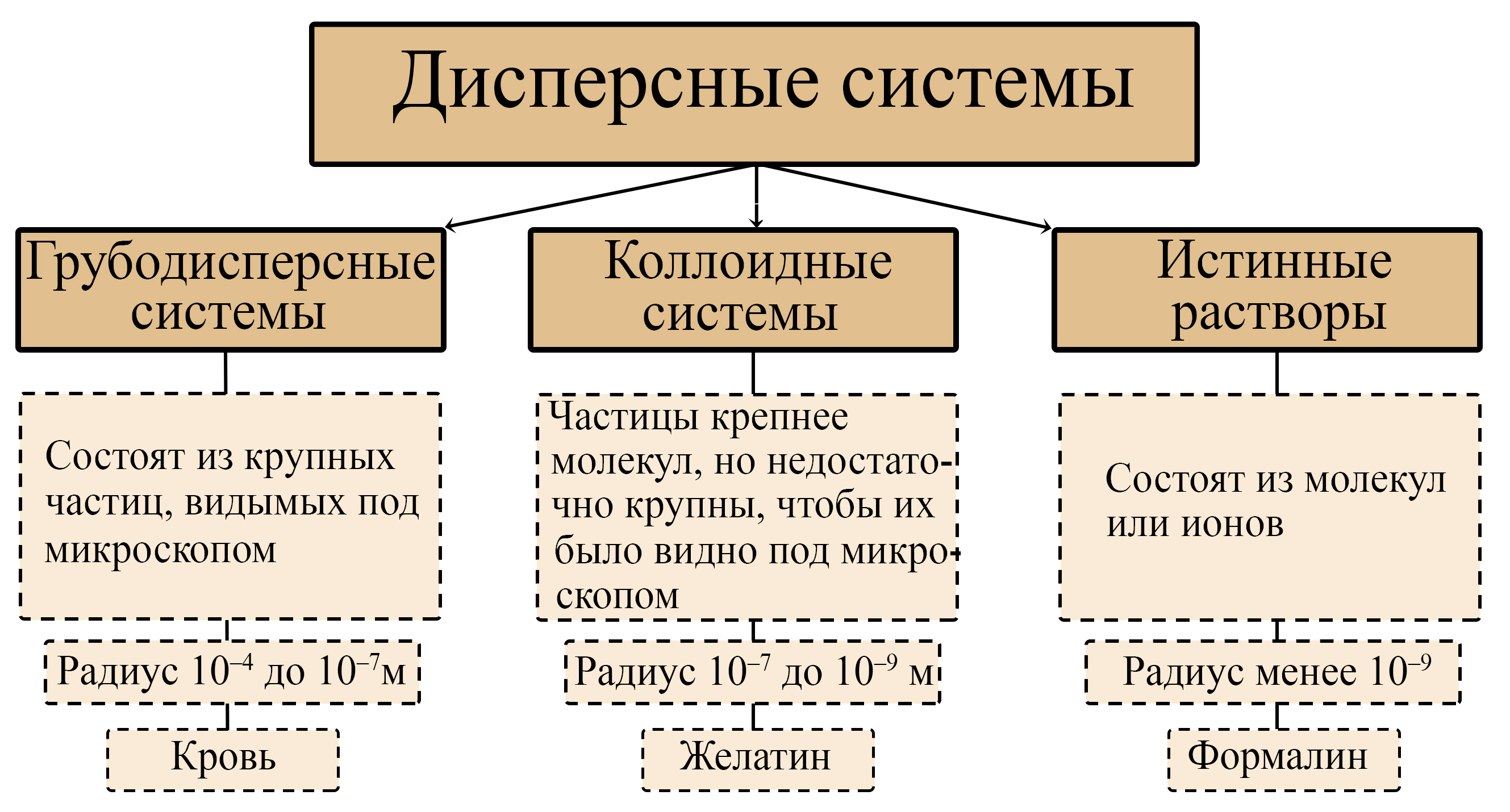 Отличия грубодисперсных и коллоидных систем от истинных растворов
Отличия грубодисперсных и коллоидных систем от истинных растворов
Классификация дисперсных систем по агрегатному состоянию
Классификация дисперсных систем по агрегатному состоянию
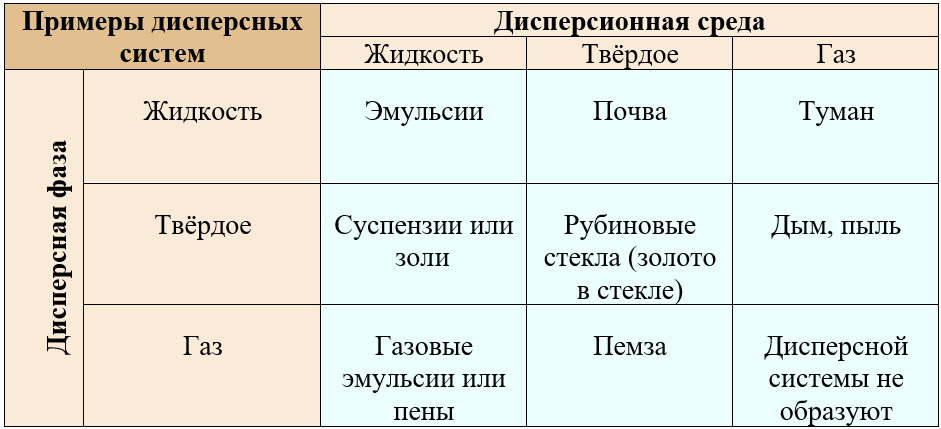 Таблица с примерами дисперсных систем в разных агрегатных состояниях
Таблица с примерами дисперсных систем в разных агрегатных состояниях
- Две или более жидкости, не смешивающиеся между собой, образуют эмульсии. При их отстаивании жидкости отслаиваются и распределяются в сосуде по плотности: более плотная жидкость опускается вниз, менее плотная жидкость поднимается наверх. В этом случае дисперсную систему восстанавливают повторным размешиванием. К эмульсиям относят масла, диспергированные в воде, например, молочные жиры в молоке, основу которого составляет вода; яичный белок, сырую нефть. Жировые эмульсии используются в медицине для инфузий (капельниц). Эмульсии широко распространены в косметологии, к ним относятся кремы. Для того чтобы компоненты эмульсии не расслаивались, используют эмульгаторы.
- Жидкость, диспергированная в газовой среде, образует туман. Примером может служит туман как погодное явление и туман, образующийся при растворении серного ангидрида или серной кислоты в воде. Этот туман обладает высокой окислительной способностью, вызывает коррозию, сжигает слизистые, поэтому данный метод получения раствора серной кислоты неприемлем. Вместо серного ангидрида используют олеум – раствор ангидрида в концентрированной серной кислоте, который растворяют не в воде, а в растворах серной кислоты, получая более концентрированные растворы. Из них, в свою очередь, можно получить раствор заданной концентрации, добавив серную кислоту в воду небольшими порциями. К системе жидкость/газ также можно отнести облака.
- Жидкость, диспергированная в твёрдом пористом веществе, образует множество природных дисперсных систем, таких как почва.
- Если мельчайшие частицы твердого вещества распределены в газовой среде, то образуется аэрозоль. Их широко применяют в быту: в форме аэрозолей выпускают дезодоранты, освежители воздуха, лекарственные средства для ингаляций.
- Если частицы твердого вещества диспергированы в жидкости, то образованная система называется суспензией, если частицы крупные или коллоидным раствором (золем), если радиус твёрды частиц не превышает 10‒7 м.
- Существуют дисперсные системы, состоящие из нескольких твёрдых веществ, например, в сырые пластмассы добавляют порошкообразные красители, пластмасса застывает и тоже становится твёрдой.
- При пропускании газа через раствор или при встряхивании раствора в резервуаре, содержащем газ (например, воздух), молекулы раствора обволакивают пузырьки газа тонким слоем, образуя пены. К таким системам относят пены моющих (поверхностно-активных) средств.
Газовая эмульсия отличается от пены тем, что в ней количество газовых частиц (дисперсной фазы) значительно меньше, чем частиц жидкости, образующих дисперсионную среду. В пене количество газовых частиц достигает 90% из-за чего пены имеют ячеистую очень рыхлую структуру.
- Газы имеют способность растворяться в твёрдых веществах. Например, водород проникает между узлами металлической решетки металлов, например, свинца. Также газы хорошо проникают между частицами силикагеля и активированного угля.
- Два газа не образуют дисперсной системы, так как при их смешивании они самопроизвольно распределяются между молекулами друг друга, и главного условия существования дисперсной системы - границы раздела фаз не наблюдается.
Коллоиды и кристаллоиды. Истинные и коллоидные растворы
Особое место в природе занимают коллоидные системы. Еще в середине XIX века шотландский ученый Томас Грэм обнаружил, что некоторые вещества, обычно не растворимые в воде, при определенных условиях могут образовывать с ней однородные смеси, отличающиеся от обычных растворов. Так, обычные растворы проходят через фильтр из растительного пергамента полностью и в дальнейшем способны кристаллизоваться, а смеси из нерастворимых веществ и воды не проходят через поры такого фильтра и не способны кристаллизоваться.
Растворы, проходящие через фильтр и способные кристаллизоваться, он назвал кристаллоидами, их принято называть истинными растворами. Смеси, не проходящие через фильтр – коллоидами, по названию клея (по греч. – «колла») или коллоидными растворами (золями). Данная классификация является простой, но устаревшей.
В истинных растворах присутствуют отдельные ионы и молекулы, тогда как в коллоидных растворах присутствуют более крупные частицы.
Классификация растворов на коллоиды и кристаллоиды
 Таблица с примерами дисперсных систем в разных агрегатных состояниях
Таблица с примерами дисперсных систем в разных агрегатных состояниях
Классификация коллоидных систем
Коллоидные системы могут быть не только жидкими (молоко, горячий раствор желатина), но и твёрдыми (яшма и многие другие окрашенные минералы), и газообразными (дым, туман).
Если дисперсионной средой выступает вода, то коллоид называется гидрозолем, если спирт – алкозоли, если бензол – бензозоли и т. д.
Если дисперсионной средой выступает газ, то коллоид называется аэрозолем.
Кроме того, существуют особые коллоиды, занимающие промежуточное состояние между жидкими и твердыми, их называют гелями. Гель образуется, например, при застывании раствора желатина при охлаждении. К гелям относят осадок кремниевой кислоты, желе, кисель.

 Селивёрстова Алиса Андреевна
Селивёрстова Алиса Андреевна  Крылова Елизавета Владимировна
Крылова Елизавета Владимировна 
 Селивёрстова Алиса Андреевна
Селивёрстова Алиса Андреевна